MECCANICA QUANTISTICA
La Meccanica Quantistica e la Teoria della Relativita' (Relativita' ristretta e Relativita' generale) si svilupparono a partire dal XX secolo, dando origine alla Fisica moderna che rivoluziono' i principi della Fisica classica.
I punti fondamentali della Fisica moderna sono:
le grandezze spazio e tempo non sono grandezze assolute, ma dipendono dal sistema di riferimento preso in esame;
c'e' equivalenza tra spazio e tempo, per cui esiste un'unica entita' omogenea denominata spazio-tempo;
la velocita' della luce e' la massima velocita' possibile nell'Universo;
coppie di grandezze fisiche, come posizione di una particella e quantita' di moto, oppure energia e tempo, non possono essere misurate simultaneamente con precisione arbitraria (principio di indeterminazione di Heisenberg);
la materia in generale presenta una doppia natura: corpuscolare ed ondulatoria.
DUALISMO ONDA - CORPUSCOLO
Contrariamente a quanto sostenuto dalla Meccanica Classica, la quale interpreta la luce solo come un'onda e l'elettrone solo come una particella, in Meccanica Quantistica la radiazione elettromagnetica e la materia vengono entrambe descritte come un fenomeno ondulatorio e come entita' particellari.
L'inaspettata e contro intuitiva proprieta' del “dualismo onda-corpuscolo” fu la ragione principale del fallimento di tutte le teorie classiche sviluppate fino al XIX secolo.
PARTICOLARI SITUAZIONI SPERIMENTALI IN CUI LA FISICA CLASSICA FALLIVA:
Radiazione di corpo nero.
Effetto fotoelettrico.
Proprieta' ondulatorie degli elettroni.
SOLUZIONI FORNITE DALLA MECCANICA QUANTISTICA:
Teoria di Planck dell'irraggiamento di un corpo nero.
Spiegazione di Einstein dell'effetto fotoelettrico.
Modello di Bohr dell'atomo di idrogeno.
Lunghezza d'onda di Louis de Broglie.
NATURA ONDULATORIA E CORPUSCOLARE DELLA LUCE E NATURA ONDULATORIA DELLA MATERIA
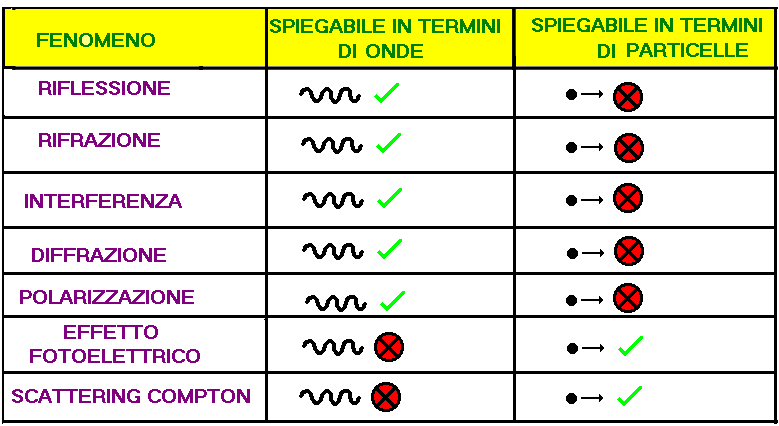
I piu' comuni fenomeni luminosi, come: riflessione, rifrazione, interferenza e diffrazione, possono essere spiegati come fenomeni ondulatori, ossia descrivendo la luce come un'onda.
Effetto fotoelettrico e Diffusione Compton dimostrano che la radiazione elettromagnetica puo' essere vista come un flusso di particelle (fotoni o quanti di luce).
La materia ed in particolare gli elettroni, che di solito sono pensati come particelle, presentano, nei fenomeni di interferenza e di diffrazione, proprieta' ondulatorie.
Schema riassuntivo riguardante la radiazione elettromagnetica:

SVILUPPO DELLA TEORIA QUANTISTICA: PUNTI CHIAVE
Max Planck ipotizza che l'energia della radiazione emessa o assorbita da un corpo nero non e' emessa e assorbita con continuita', ma in quantita' discrete (quanti) di valore E = hʋ con h (costante di Planck) = 6,63 × 10-34 J·s = 6,63 x 10-27 erg·s e ʋ = frequenza di oscillazione.
Albert Einstein riconosce per primo che la quantizzazione dell'energia della radiazione emessa o assorbita e' una proprieta' generale della radiazione elettromagnetica, pensando ad essa come ad un insieme di fotoni di energia E = hʋ.
Niels Bohr applica le idee di Einstein, riguardanti la quantizzazione dell'energia, all'energia di un atomo. Egli propone un modello per l'atomo di idrogeno che si rivela un successo spettacolare nei calcoli delle lunghezze d'onda della radiazione emessa dall'idrogeno.
Louis de Broglie sostiene per primo la natura ondulatoria della materia. La sua relazione λ = h/p lega la quantita' di moto p di una particella alla lunghezza λ di un'onda. Questa relazione, unita all'espressione di Bohr della quantizzazione del momento angolare (mvr = nh/2π), porta alla condizione riguardante la formazione di onde stazionarie sull'orbita elettronica in un atomo. In sostanza, le orbite permesse ad un elettrone in un atomo, nel suo moto intorno al nucleo, dovevano essere soltanto quelle stazionarie, ossia quelle contenenti un numero intero n di lunghezze d'onda λ di de Broglie (2πr = nλ = C dove C e' la circonferenza dell'orbita di Bohr). Con questo risultato e' stato possibile considerare la quantizzazione dell'energia una conseguenza della natura ondulatoria delle particelle materiali.
Erwin Schrödinger tratta matematicamente le onde di Louis de Broglie e giunge ad un'equazione differenziale. La sua equazione, in riferimento a particelle vincolate (cioe' soggette a forze, come sono gli elettroni in un atomo), ammetteva soluzioni solo nel caso in cui l'energia delle particelle assumeva dei valori ben precisi. Con la soluzione della sua equazione (la funzione d'onda Ψ di una particella) Schrödinger giunge a definire lo stato energetico degli elettroni in accordo con gli stati energetici indicati da Bohr.
Born fornisce l'interpretazione fisica di funzione d'onda come onda di probabilita'; cio' porta successivamente al concetto di orbitale inteso come: “zona attorno al nucleo in cui la probabilita' di trovare l'elettrone risulta molto alta”. Si trattava di un concetto piu' avanzato e sottile rispetto a quello delle orbite di Bohr.
Bohr proponeva un modello atomico nel quale gli elettroni erano paragonabili a piccoli pianeti in rotazione intorno al nucleo, con un raggio dell'orbita ed un impulso ben definiti, violando cosi' il principio di indeterminazione di Heisenberg secondo il quale posizione ed impulso di una particella non potevano essere determinati contemporaneamente con precisione arbitraria.
Grazie a Schrödinger e a Born si giunse ad una conoscenza piu' approfondita dell'atomo e si pote' costruire un nuovo modello atomico il modello atomico ad orbitali, piu' completo ed efficace del modello atomico di Bohr.
Il concetto di funzione d'onda, introdotto da Schrödinger, sostitui' quello di traiettoria precisa di una particella e fu considerato il principale concetto della Teoria Quantistica.

MECCANICA CLASSICA E MECCANICA QUANTISTICA A CONFRONTO
MECCANICA CLASSICA: teoria fisica di natura deterministica, cioe' basata sul principio di causalita'. In pratica, grazie alle scoperte di Newton e di Galileo Galilei, conoscendo le proprieta' di un corpo (massa, forma, ecc.), le sue condizioni iniziali di moto (posizione, velocita', ecc.) e le condizioni esterne (campi di forze, ecc.), e' possibile determinare, in modo esatto, il comportamento del corpo istante per istante. Quindi, in natura, nulla avviene per caso, ma ogni evento e' determinato da una causa ben precisa.
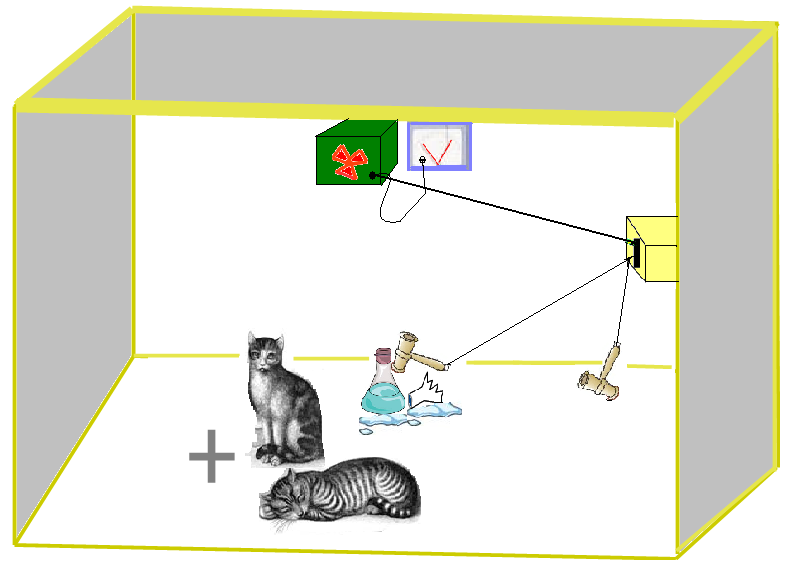
MECCANICA QUANTISTICA: teoria fisica di natura probabilistica, cioe' basata sul concetto di probabilita' e di osservazione. Il famoso esempio del gatto di Schrödinger chiarisce la natura della Meccanica Quantistica.
In questo esempio un gatto e' chiuso in una scatola, nella quale vi e' un macchinario collegato ad una boccetta contenente del veleno. Il macchinario si avvia quando un elemento radioattivo decade, rompendo la boccetta di veleno. Dall'esterno, il gatto, dentro la scatola, puo' essere “vivo” o “morto”, in quanto non si sa se l'elemento radioattivo sia decaduto oppure no. Dunque, per la Meccanica Quantistica il gatto e' “sia vivo che morto”, si dice che e' in una “sovrapposizione di stati” (stato “vivo” e stato “morto”). Soltanto la fase di osservazione congela lo stato del gatto, determinandone la sorte.
IL PIU' IMPORTANTE ESPERIMENTO SCIENTIFICO DEL XX SECOLO
Si tratta dell'esperimento di Teletrasporto quantistico, effettuato per la prima volta nel 1997. Questo esprimento dimostra come particelle entangled, ossia “correlate”, possano comunicare istantaneamente tra loro nel tempo e nello spazio, indipendentemente dalla loro distanza.
La condizione di entanglement, relativa a due particelle, fu dimostrata nel 1982 dal fisico Alain Aspect, in collaborazione con i ricercatori J.Dalibard e G.Roger dell'Istituto di Ottica dell'Universita' di Parigi.
Questo tipo di comunicazione quantistica implicherebbe la non esistenza delle dimensioni comunemente percepite sotto forma di “spazio” e di “tempo”; ogni cosa avverrebbe nello stesso punto e nello stesso momento e la comune percezione del passato e delle distanze sarebbe solo una pura illusione.